phản tốt, tuy nhiên, chế độ này chỉ có thể thực hiện khi mẫu đủ mỏng và quang sai của kính đủ nhỏ cho phép [118]. Trong luận án này, ảnh TEM cho phép xác định kích thước các hạt oxit phức hợp của Cu và Mn sau tổng hợp.
2.3.3.3. Phương pháp nhiễu xạ tia X (X-ray)
Phương pháp này sử dụng để phân tích cấu trúc tinh thể của các oxit sau khi tổng hợp. Tinh thể là sự hợp thành của một tập hợp khối các nguyên tố đồng nhất gọi là mắt xích. Nó bao gồm một hoặc nhiều nguyên tố khác nhau. Người ta có thể xác định những mặt phẳng song song và cách đều đi qua những nguyên tử, những mặt phẳng này gọi là sơ đồ mạng tinh thể.
Một chuỗi những mặt phẳng được xác định bằng khoảng cách giữa các mặt phẳng của mạng dhkl (khoảng cách giữa hai mặt phẳng song song).
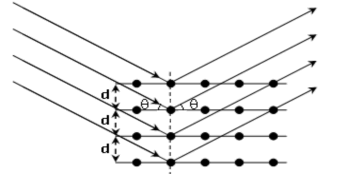
Hình 2.1. Hiện tượng các tia X nhiễu xạ trên các mặt tinh thể chất rắn Phương pháp nhiễu xạ tia X là phương pháp phân tích không phá hủy
mẫu. Các định hướng của nhiễu xạ chỉ phụ thuộc vào mạng lưới tinh thể, vị trí của các nguyên tử trong mạng lưới chỉ liên quan đến giá trị của biên độ và cường độ nhiễu xạ. Nói cách khác, tất cả những tinh thể có cùng cấu trúc mạng thì có cùng sự định hướng nhiễu xạ.
Khi có sự nhiễu xạ chiếu vào bề mặt mẫu, sẽ tạo ra một quan hệ (hệ thức Bragg) giữa khoảng cách dhkl của hai mặt phẳng mạng và góc tới như sau:
p = 2 dhkl sin (2.1)
Với: : bước sóng của bức xạ X tới p: tổng số bậc nhiễu xạ
Hệ thức trên cho phép xác định được sơ đồ mạng phản xạ lại của tia X. Đối với một tinh thể, sự khuếch tán gần như gián đoạn, vì vậy giản đồ phổ nhiễu xạ tia X biểu thị mối quan hệ giữa cường độ nhiễu xạ theo hàm của góc 2, cho ra những vạch phổ đặc trưng.
Phổ nhiễu xạ tia X được thực hiện trên thiết bị Diffractemrter Philips 1380, phát tia bằng cực Mo, năng lượng 30 KeV, bước sóng kích thích = 0,7093Ao.
2.3.3.4. Phương pháp phổ tử ngoại khả kiến (UV-Vis) [19]
Phương pháp này cho biết sự phụ thuộc của cường độ hấp thụ A vào nồng độ chất cần phân tích theo phương trình 2.2.
A = lg I0
I
= l C (2.2)
Trong đó: A: cường độ hấp thụ.
l : chiều dày lớp chất hấp thụ (cuvet), tính bằng cm. C : nồng độ chất hấp thụ, tính ra mol/l.
: Hệ số hấp thụ mol.
Từ đó có thể đánh giá hiệu suất phân hủy hợp chất màu azo qua cường độ hấp thụ theo công thức 2.3.

(2.3)
Trong đó: : Hiệu suất phân hủy (%)
A0: Cường độ hấp thụ tại thời điểm ban đầu At: Cường độ hấp thụ tại thời điểm t
Ngoài ra, phương pháp này cho phép xây dựng đường chuẩn nồng độ - cường độ để nghiên cứu sự biến thiên nồng độ của hợp chất azo trong quá trình khoáng hóa. Để xây dựng đường chuẩn, cần pha một dãy dung dịch chuẩn có nồng độ khác nhau, với dung môi pha loãng là dung dịch Na2SO4 0,05 M, pH3, sau đó đo cường độ hấp thụ UV-Vis của các dung dịch.
2.3.3.5. Phương pháp xác định nhu cầu oxy hóa học (COD)
Trong đề tài luận án này, COD được xác định bằng phương pháp đicromat với xúc tác Ag2SO4, cách tiến hành như sau:
Dùng pipet hút 2 ml mẫu cho vào ống nghiệm, thêm 3 ml H2SO4 98 %,
1 ml K2Cr2O7 0,05 N, lắc đều. Sau đó ủ trong 2 giờ ở 150oC. Để nguội, chuẩn độ với dung dịch muối mo (sắt amoni sunphat), thêm chính xác 1 giọt chỉ thị điphenylamin 1 %, dừng chuẩn độ khi dung dịch chuyển từ màu tím đen sang màu xanh rêu có ánh vàng.
Nhu cầu oxy hóa học được tính theo công thức:
COD (a b) * N *8*1000(mg / l) V
(2.4)
Với a: Thể tích dung dịch muối mo dùng chuẩn độ mẫu trắng (ml)
b: Thể tích dung dịch muối mo dùng để chuẩn độ mẫu cần xác định COD (ml) N: Nồng độ đương lượng của dung dịch muối mo (N)
V: Thể tích dung dịch mẫu đem chuẩn độ (ml)
Lượng chất hữu cơ bị oxy hóa được đánh giá bằng độ suy giảm chỉ số COD trước và sau xử lý (COD).
Hiệu suất dòng điện trong quá trình điện phân được tính theo công thức:
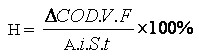 (2.5
(2.5
i: mật độ dòng điện (A/cm2) S: diện tích bề mặt điện cực (cm2) t: thời gian oxy hóa (giây) A: số đương lượng của oxi, A = 8 |
Có thể bạn quan tâm!
-
 Sự Chuyển Động Của Các Sóng Âm Liên Quan Đến Sự Phát Triển Và Nổ Của Các Bọt Khí.
Sự Chuyển Động Của Các Sóng Âm Liên Quan Đến Sự Phát Triển Và Nổ Của Các Bọt Khí. -
![Dự Đoán Cơ Chế Của Phản Ứng Khoáng Hóa Azobenzen Bằng Hiệu Ứng Fenton Điện Hóa [83]](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Dự Đoán Cơ Chế Của Phản Ứng Khoáng Hóa Azobenzen Bằng Hiệu Ứng Fenton Điện Hóa [83]
Dự Đoán Cơ Chế Của Phản Ứng Khoáng Hóa Azobenzen Bằng Hiệu Ứng Fenton Điện Hóa [83] -
 Sơ Đồ Phân Tán Chất Xúc Tác Điện Hóa Trong Màng Polyme Dẫn Cấu Trúc Xốp Và Diện Tích Bề Mặt Lớn Của Nhiều Loại Polyme Dẫn Đã Tạo
Sơ Đồ Phân Tán Chất Xúc Tác Điện Hóa Trong Màng Polyme Dẫn Cấu Trúc Xốp Và Diện Tích Bề Mặt Lớn Của Nhiều Loại Polyme Dẫn Đã Tạo -
 Bảng So Sánh Chỉ Số Mặt Phẳng Mạng Tinh Thể (Hkl) Của Oxit Phức Hợp Của Cu Và Mn, Oxit Spinel Và Cuo
Bảng So Sánh Chỉ Số Mặt Phẳng Mạng Tinh Thể (Hkl) Của Oxit Phức Hợp Của Cu Và Mn, Oxit Spinel Và Cuo -
 Kết Luận Về Tổng Hợp Và Đặc Tính Của Màng Ppy Và Ppy(Oxit)/ppy:
Kết Luận Về Tổng Hợp Và Đặc Tính Của Màng Ppy Và Ppy(Oxit)/ppy: -
 Các Đường Cong Phân Cực Catôt Trên Điện Cực Cacbon.
Các Đường Cong Phân Cực Catôt Trên Điện Cực Cacbon.
Xem toàn bộ 165 trang tài liệu này.
Hiệu suất suy giảm COD trong quá trình khoáng hóa được tính theo công thức sau: %COD = COD*100%/CODo .
2.3.3.6. Phương pháp đo độ màu
Trong đề tài luận án, độ màu của nước thải trước và sau xử lý được đo tại Viện Công nghệ môi trường - Viện Hàn lâm Khoa học và Công nghệ Việt Nam.
2.3.3.7. Phương pháp khảo sát, điều tra:
- Mục đích: Trong luận án này, phương pháp khảo sát, điều tra được áp dụng nhằm xác định các loại thuốc nhuộm sử dụng trong quá trình sản xuất dệt nhuộm tại các làng nghề dệt nhuộm Dương Nội và Vạn Phúc.
- Các bước thực hiện:
+ Tiếp cận các cơ sở sản xuất;
+ Tìm hiểu các loại thuốc nhuộm thường dùng;
+ Tra cứu để tìm ra cấu trúc của các loại thuốc nhuộm.
CHƯƠNG 3. KẾT QUẢ VÀ THẢO LUẬN
3.1. Đặc tính của oxit phức hợp của Cu và Mn
3.1.1. Hình thái bề mặt
Oxit phức hợp của Cu và Mn thu được có dạng bột mịn, màu xám đen. Cấu trúc bề mặt của các hạt oxit được xác định bằng phương pháp kính hiển vi điện tử quét (SEM) (hình 3.1).
Từ ảnh SEM có thể thấy: Các tinh thể trên bề mặt oxit sau tổng hợp có kích thước khá đồng đều. Tuy nhiên, do ảnh SEM chỉ cho phép quan sát các tinh thể trên bề mặt nên khó đánh giá được kích thước của các hạt oxit riêng biệt. Để khắc phục hạn chế này, các oxit phức hợp đã được quan sát bằng kính hiển vi điện tử truyền qua (TEM).
Một lượng rất nhỏ bột oxit được phân tán đều trong cồn dưới dạng huyền phù nhờ siêu âm. Dung dịch huyền phù được nhỏ lên lưới đồng rất mỏng, sấy nhẹ cho đến khô và quan sát bằng kính hiển vi điện tử truyền qua. Ảnh TEM của oxit phức hợp được thể hiện trên hình 3.2a.

Hình 3.1. Ảnh SEM của oxit phức hợp của Cu và Mn

Ảnh nhiễu xạ điện tử (b) |
Hình 3.2. Ảnh TEM của oxit phức hợp của Cu và Mn
Quan sát ảnh TEM (hình 3.2a), có thể nhận thấy, oxit sau tổng hợp tồn tại dưới dạng hạt với kích thước tương đối lớn (khoảng vài trăm nanomet).
Ảnh nhiễu xạ điện tử của oxit sau tổng hợp được thực hiện đồng thời trên thiết bị chụp TEM (hình 3.2b) cho đường tròn đồng tâm, chứng tỏ oxit sau tổng hợp tạo thành có cấu trúc tinh thể.
3.1.2. Thành phần của oxit
Phổ tán xạ năng lượng tia X là phương pháp phân tích định tính chính xác. Bằng phương pháp này, có thể xác định được thành phần các nguyên tố có mặt trong các oxit. Bên cạnh đó, cũng có thể định lượng được thành phần của các nguyên tố “nặng” có số hiệu nguyên tử Z > 10 trong bảng hệ thống tuần hoàn. Các kết quả phân tích thành phần hoá học của oxit sau tổng hợp bằng phổ tán xạ năng lượng tia X được biểu diễn trên hình 3.3 và bảng 3.1.
Kết quả phân tích cho thấy thành phần của oxit sau tổng hợp tương đối “sạch”. Ngoài các pic của Cu, Mn và O còn có các pic đặc trưng của S với hàm lượng rất nhỏ, nguyên nhân có thể do S còn lưu lại trong quá trình tổng hợp oxit bằng phương pháp đồng kết tủa đi từ CuSO4 và MnSO4.
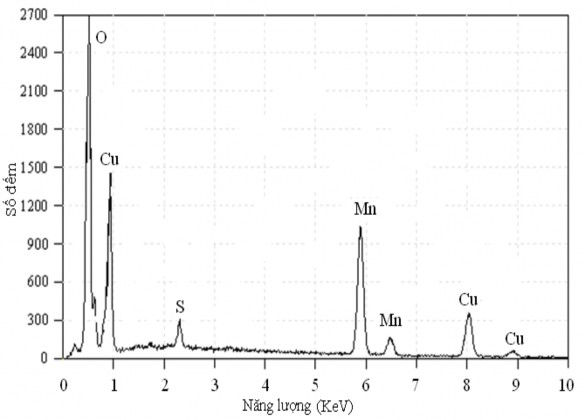
Hình 3.3. Phổ tán xạ năng lượng tia X của oxit phức hợp của Cu và Mn
Bảng 3.1. Thành phần các nguyên tố trong oxit phức hợp của Cu và Mn
% về khối lượng | % về nguyên tử | |
Cu | 40,12 | 24,11 |
Mn | 38,49 | 26,75 |
S | 1,78 | 2,12 |
O | 18,19 | 43,42 |
Các tạp chất khác | 1,42 | 3,6 |
Total | 100 | 100 |
Kết quả phân tích định lượng các nguyên tố cho biết, trong oxit sau tổng hợp, tỉ lệ theo số mol Cu : Mn 1 : 1.
3.1.3. Cấu trúc tinh thể
Cấu trúc tinh thể của oxit sau tổng hợp được xác định bằng phương pháp phổ nhiễu xạ tia X (hình 3.4).
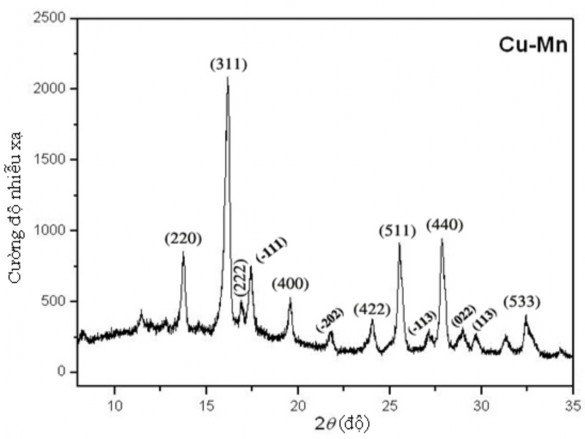
Hình 3.4. Phổ nhiễu xạ tia X của oxit phức hợp của Cu và Mn
So sánh với phổ chuẩn của oxit spinel (hình 3.5) có thể thấy, phổ nhiễu xạ tia X của oxit sau tổng hợp có xuất hiện các pic đặc trưng của oxit spinel. Ngoài ra, trên phổ nhiễu xạ tia X của oxit sau tổng hợp còn có xuất hiện một số pic “lạ” có cường độ rất nhỏ (-111), (-202), (-113), (113), (022), không đặc trưng cho cấu trúc spinel. So sánh với phổ chuẩn của đồng(II) oxit (bảng 3.2) cho phép dự đoán rằng, ngoài thành phần chính (oxit spinel) còn có một lượng nhỏ đồng(II) oxit tồn tại dưới dạng monoclinic. Ngoài ra, còn một số pic khác, có thể tương ứng với cấu trúc của mangan oxit.
Dựa vào kết quả từ phổ nhiễu xạ tia X cho phép khẳng định oxit sau tổng hợp có thành phần cơ bản là oxit spinel và có công thức phân tử dạng


![Dự Đoán Cơ Chế Của Phản Ứng Khoáng Hóa Azobenzen Bằng Hiệu Ứng Fenton Điện Hóa [83]](https://tailieuthamkhao.com/uploads/2022/05/09/nghien-cuu-dac-diem-cua-qua-trinh-khoang-hoa-mot-so-hop-chat-huu-co-ho-6-1-120x90.jpg)