DANH MỤC HÌNH ẢNH
Hình 1.1. Mô tả quá trình hình thành nano silica xốp, biến tính và mang thuốc 5
Hình 1.2. Quá trình hình thành hạt nano silica cấu trúc xốp 6
Hình 1.3. Nguyên lý tạo hạt silica bằng phương pháp CVC 7
Hình 1.4. Sự tạo thành Chitosan từ Chitin 10
Có thể bạn quan tâm!
-
 Nghiên cứu biến tính bề mặt nano silica làm chất mang thuốc chống ung thư - 1
Nghiên cứu biến tính bề mặt nano silica làm chất mang thuốc chống ung thư - 1 -
 Mô Tả Quá Trình Hình Thành Nano Silica Xốp, Biến Tính Và Mang Thuốc
Mô Tả Quá Trình Hình Thành Nano Silica Xốp, Biến Tính Và Mang Thuốc -
 Tổng Hợp Nano Silica Xốp (Pns) Bằng Phương Pháp Ngưng Tụ Hóa Học (Chemical Vapor Condensation Gọi Tắt Là Cvc)
Tổng Hợp Nano Silica Xốp (Pns) Bằng Phương Pháp Ngưng Tụ Hóa Học (Chemical Vapor Condensation Gọi Tắt Là Cvc) -
 Ứng Dụng Công Nghệ Nano Làm Chất Dẫn Truyền Thuốc Chống Ung Thư
Ứng Dụng Công Nghệ Nano Làm Chất Dẫn Truyền Thuốc Chống Ung Thư
Xem toàn bộ 137 trang tài liệu này.
Hình 1.5. Cấu trúc hóa học của 3,3’-dithiodipropionic acid 11

Hình 1.6. Liên kết disulfide ban đầu bị cắt đứt và tái hình thành liên kết disulfide khác ... 11 Hình 1.7. Cấu trúc cơ bản của Gelatin 13
Hình 1.8. Công thức của Fluorouracil (5-FU) 14
Hình 1.9. Công thức hóa học của Fluorouracil (5-FU) và cơ chế tiêu diệt tế bào ung thư của 5-FU 14
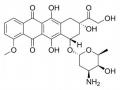
Hình 1.10. Công thức cấu tạo của doxorubicin 15
Hình 1.11. Nhắm mục tiêu thụ động 18
Hình 1.12. Thành tựu nghiên cứu khoa học trong lĩnh vực dẫn truyền thuốc 19
Hình 1.13. Cơ chế phản ứng thủy phân và ngưng tụ 20
Hình 1.14. Cấu trúc 3-glycidoxypropyltrimethoxysilane 21
Hình 1.15. Phản ứng tạo cầu nối GPTMS trên nano silica xốp (PNS-GPTMS) 21
Hình 1.16. Phản ứng tạo cầu nối APTES trên nano silica xốp (PNS-APTES) 22
Hình 1.17. Phản ứng biến tính nano silica xốp(PNS) bằng hydrazine 22
Hình 1.18. Phản ứng tổng hợp mPEG-p-nitrophenyl carbonate 23
Hình 1.19. Phản ứng tổng hợp chitosan-mPEG 23
Hình 1.20. Phản ứng biến tính nano silica bởi Chitosan-mPEG 24
Hình 1.21. Phản ứng tạo gắn anhidride succinic lên PNS (PNS-APTES-COOH) 24
Hình 1.22. Phản ứng hoạt hóa PNS-APTES-Succinic bằng EDC 25
Hình 1.23. Phản ứng tạo liên kết PNS-APTES-Anhydride succinic với gelatin 25
Hình 1.24. Phản ứng tổng hợp gelatin-mPEG. 27
Hình 1.25. Phản ứng tạo liên kết PNS-APTES-Anhydride succinic với Gelatin-mPEG 27
Hình 1.26. Phản ứng tạo PNS-SS-COOH 28
Hình 1.27. Phản ứng hoạt hóa PNS-SS-COOH với EDC 28
Hình 1.28. Phản ứng tổng hợp chất mang thuốc PNS@CS-PEG 29
Hình 2.1. Mô tả qui trình tổng hợp porous nano silica (PNS) 31
Hình 2.2. Sơ đồ qui trình tổng hợp nano silica xốp (PNS) bằng phương pháp sol-gel 32
Hình 2.3. Qui trình tổng hợp nano silica xốp (PNS) bằng phương pháp kết tủa 33
Hình 2.4. Qui trình tổng hợp PNS-GPTMS 34
Hình 2.5. Sơ đồ tổng hợp PNS-APTES 35
Hình 2.6. Quy trình tổng hợp PNS-GPTMS-Hydrazine 36
Hình 2.7. Hoạt hóa mPEG bằng NPC 37
Hình 2.8. Qui trình tổng hợp Chitosan-mPEG 38
Hình 2.9. Qui trình tổng hợp PNS-GPTMS-CS-mPEG. 39
Hình 2.10. Quy trình tổng hợp PNS-APTES-succinic anhydrid 39
Hình 2.11. Qui trình tổng hợp PNS-APTES-COOH-GE 40
Hình 2.12. Hoạt hóa mPEG bằng NPC 41
Hình 2.13. Qui trình tổng hợp Gelatin-mPEG 42
Hình 2.14. Qui trình tổng hợp PNS-APTES-COOH-GEL-mPEG 43
Hình 2.15. Sơ đồ quy trình mang 5-FU 46
Hình 2.16. Sơ đồ quy trình mang DOX 47
Hình 3.1. Ảnh hưởng của TEOs lên kích thước hạt 50
Hình 3.2. Ảnh hưởng của ethanole lên kích thước hạt 50
Hình 3.3. Ảnh hưởng của nồng độ amoniac lên kích thước hạt 51
Hình 3.4. Ảnh TEM và phân bố kích thước hạt của nanosilica xốp (PNS) 51
Hình 3.5. Ảnh SEM của nano silica xốp (PNS) tổng hợp bằng phương pháp kết tủa 52
Hình 3.6. So sánh giản đồ XRD của nano silica xốp tổng hợp bằng phương pháp kết tủa (a) và bằng phương pháp sol-gel (b). 53
Hình 3.7. So sánh phổ FT-IR của nano silica xốp (PNS) tổng hợp bằng phương pháp sol-gel và bằng phương pháp kết tủa 54
Hình 3.8. Ảnh TEM của PNS-GPTMS (A, A’) và PNS-GPTMS-Hydrazine (B, B’) 56
Hình 3.9. FTIR của PNS (a), PNS-GPTMS(b) và PNS-GPTMS-Hydrazine (c) 57
Hình 3.10. Ảnh TEM của PNS-GPTMS-CS-mPEG 57
Hình 3.11. Kết quả FTIR của a) Nano silica xốp (PNS); b)PNS-GPTMS; c) PNS-GPTMS – Cs-mPEG; d) Cs-mPEG 58
Hình 3.12. Giản đồ TGA của PNS-GPTMS (a) và PNS-GPTMS-Cs-mPEG (b) 59
Hình 3.13. FTIR của (a) PNS, (b) PNS-APTES, (c) PNS-APTES-COOH, (d) PNS-APTES- COOH-GE 61
Hình 3.14. Ảnh TEM của vật liệu nano silicate sau khi biến tính bằng gelatin 61
Hình 3.15. Ảnh TEM, sơ đồ phân bố kích thước hạt của vật liệu nano silicate trước biến tính(a,b) và sau biến tính bằng GEL-mPEG (c,d) 62
Hình 3.16. Giản đồ XRD góc nhỏ của (a) PNS (CTAB), (b) PNS-COOH, and (c) PNS- GEL-mPEG 63
Hình 3.17. FTIR của (a) PNS, (b) PNS-APTES, (c) PNS-APTES-COOH, (d) GEL-mPEG, and (e) PNS-GEL-mPEG 64
Hình 3.18. Giản đồ TGA của PNS; PNS-APTES-COOH; GEL-mPEG và PNS-GPTMS- GEL-mPEG 65
Hình 3.19. Đường đẳng nhiệt hấp phụ BET của hệ PNS-GPTMS-GEL-mPEG 65
Hình 3.20. Ảnh TEM của vật liệu PNS@CS-PEG và sơ đồ phân bố kích thước hạt 66
Hình 3.21. FT-IR của (a) PNS và (b) PNS@CS-PEG 67
Hình 3.22.Đồ thị tương quan giữa diện tích bề mặt (BET) và kích thước hạt (TEM) của hệ PNS trước và sau biến tính 68
Hình 3.23. Đường chuẩn 5-FU 69
Hình 3.24. Đường chuẩn thuốc DOX 70
Hình 3.25. Tỉ lệ giữa thuốc và chất mang 71
Hình 3.26. Phổ HPLC của 5-FU (a) và HPLC của hệ PNS mang 5-FU giải phóng (b) 72
Hình 3.27. Đồ thị mô tả khả năng giải phóng thuốc DOX của hệ PNS ở pH 4,5 và pH 7,4
.............................................................................................................................................. 74
Hình 3.28. HPLC của 5-FU (a) và HPLC của hệ PNS-Hydrazine mang 5-FU giải phóng (b)
.............................................................................................................................................. 75
Hình 3.29. Đồ thị mô tả khả năng giải phóng thuốc DOX của hệ PNS-Hydrazine ở pH 4,5 và pH 7,4 78
Hình 3.30. Quá trình giải phóng thuốc DOX của hệ PNS-Hydrazine ở pH 4,5 và pH 7,4
.............................................................................................................................................. 78
Hình 3.31. Phổ HPLC của 5-FU (a) và HPLC của hệ PNS-GPTMS-CS-mPEG mang 5-FU giải phóng (b) 80
Hình 3.32. Đồ thị mô tả khả năng giải phóng thuốc DOX của hệ PNS-GPTMS-CS-mPEG
.............................................................................................................................................. 82
Hình 3.33. Phổ HPLC của 5-FU (a) và HPLC của hệ PNS-APTES mang 5-FU giải phóng (b) 84
Hình 3.34. Đồ thị mô tả khả năng giải phóng của PNS-APTES 85
Hình 3.35. Phổ HPLC của 5-FU (a) và HPLC của hệ PNS-APTES-COOH-GE mang 5-FU giải phóng (b) 88
Hình 3.36. Đồ thị so sánh khả năng giải phóng DOX của PNS-APTES-COOH-GE 89
Hình 3.37.Phổ HPLC của 5-FU (a) và HPLC của hệ PNS-GEL-mPEG mang 5-FU giải phóng (b) 90
Hình 3.38. So sánh giải phóng DOX của PNS và PNS-GEL-mPEG tại pH 7,4 và 4,5 ... 92 Hình 3.39. Đồ thị so sánh khả năng DOX của PNS và PNS-GEL-mPEG tại pH 7,4 94
Hình 3.40. So sánh giải phóng DOX của PNS@CS-PEG tại pH 7,4 và 4,5 95
Hình 3.41. Hoạt tính ức chế tế bào MCF-7 (ung thư vú) của (a) DOX và (b) PNS-APTES- COOH-GE mang DOX 99
DANH MỤC BẢNG
Bảng 2.1. Tên hóa chất và nơi xuất xứ 30
Bảng 3.1. Số liệu tương quan giữa diện tích bề mặt (BET) và kích thước hạt (TEM) của hệ PNS trước và sau biến tính 67
Bảng 3.2. Số liệu đường chuẩn thuốc 5-FU 69
Bảng 3.3. Số liệu đường chuẩn thuốc DOX 70
Bảng 3.4. Số liệu khảo sát tỷ lệ giữa thuốc DOX và chất mang 70
Bảng 3.5. Kết quả giải phóng DOX của hệ PNS 73
Bảng 3.6. Số liệu biểu thị khối lượng thuốc được mang trong 60 mg hạt 74
Bảng 3.7. So sánh DLE và DLC của PNS và PNS-GPTMS-Hydrazine mang thuốc 5FU . 75 Bảng 3.8. Kết quả giải phóng DOX của hệ PNS GPTMS-Hydrazine 77
Bảng 3.9. Lượng thuốc 5-FU tự do của hệ PNS-GPTMS-CS-mPEG 79
Bảng 3.10. Kết quả đo thuốc DOX tự do của hệ PNS-GPTMS-CS-mPEG 81
Bảng 3.11. So sánh số liệu DLE và DLC của PNS-GPTMS-CS-mPEG và PNS 81
Bảng 3.12. Dữ liệu cho thấy khả năng giải phóng thuốc DOX của hệ PNS-GPTMS-CS- mPEG ở pH=7,4 và pH=4,5 81
Bảng 3.13. Khối lượng thuốc tự do và được mang trong 60 mg chất mang PNS-APTES 83
Bảng 3.14. Hiệu suất mang thuốc và khả năng chứa thuốc 5-FU của hạt nano silica xốp đã biến tính (PNS-APTES) so sánh với PNS chưa biến tính 83
Bảng 3.15. Số liệu giải phóng DOX của PNS-APTES tại pH 7,4 và 4,5 85
Bảng 3.16. Kết quả đo dung dịch A và B (trước và sau mang thuốc 5-FU của hệ PNS- APTES-Anhydrid Succinic-GE) 87
Bảng 3.17. Số liệu giải phóng DOX của hệ PNS- APTES-COOH-GE tại pH 7,4 và 4,5... 88
Bảng 3.18. Số liệu biểu thị khối lượng thuốc 5-FU được mang trong 60 mg PNS-GEL- mPEG 90
Bảng 3.19. Khả năng giải phóng DOX của hệ PNS-GEL-mPEG ở pH=7,4 và pH=4,5 91
Bảng 3.20. So sánh khả năng giải phóng DOX của hệ PNS và PNS-GEL-mPEG ở pH=7,4
..................................................................................................................................... 93
Bảng 3.21. Dữ liệu cho thấy khả năng giải phóng thuốc DOX của hệ PNS@CS-PEG ở pH=7,4 và pH=4,5 95
Bảng 3.22. So sánh hiệu suất mang thuốc và khả năng giải phóng thuốc DOX của PNS và các hệ PNS biến tính 97
Bảng 3.23. So sánh hiệu suất mang thuốc và khả năng giải phóng 5-FU của PNS và các hệ PNS biến tính 98
Bảng 3.24. Giá trị IC50 của chất mang DOX và DOX tự do trên các dòng tế bào 99
DANH MỤC KÝ HIỆU VÀ CHỮ VIẾT TẮT
Từ viết tắt Từ viết đầy đủ
APTES (3-aminopropyl)triethoxysilane
CTAB Cetyltrimethylamnonium bromide
CS Chitosan
GEL hoặc GE Gelatin
Da Dalton
DOX Doxorubicin
5-FU Fluorouracil
DLS Dynamic light scattering
EDC 1-3 Dimethylamino-5-ethyl carbodimide
Et Ethyl
EtOH Ethanol
FT-IR Fourier transform infrared spectroscopy (phổ hồng ngoại)
Gelatin GEL hoặc GE
mPEG Methoxy ethyleneglycol
MSN Nano silica mesoporous
NPC p-nitrophenyl carbonate
PEG Poly ethyleneglycol
PNS Porous nano silicas
PBS Phosphate buffered saline
TEOS Tetraethyl orthosilicate
THF Tetrahydrofuran
TGA Thermogravimetric analysis
TEM Transmission electron microscopy
UV-Vis Ultraviolet-visible
XRD X-ray powder diffraction
Theo đánh giá thống kê của GLOBOCAN năm 2020, tình hình mắc và tử vong do ung thư trên toàn thế giới có xu hướng tăng. Việt Nam là quốc gia có tỷ lệ mắc ung thư thuộc loại cao trên thế giới, ước tính có 182 563 ca mắc mới và 122 690 ca tử vong do ung thư. Vậy cứ 100 000 người thì có 159 người chẩn đoán mắc ung thư và 106 người tử vong do ung thư (nội dung trích từ cổng thông tin điện tử của Bộ Y tế). Ung thư đem lại gánh nặng cho nền kinh tế quốc gia.
Việc chữa trị bệnh ung thư với các phương pháp khác nhau như phẫu thuật, xạ trị, hóa trị liệu, sinh trị liệu,… nhưng phổ biến hơn là hóa trị liệu. Sử dụng hóa chất trong điều trị ung thư có ưu điểm là tiêu diệt tế bào ung thư đang phát triển và nhân lên nhanh chóng, làm cho khối u ung thư dần bị suy thoái. Nhưng các tác dụng phụ của phương pháp hóa trị theo cách truyền thống là cực kỳ nguy hiểm cho bệnh nhân. Cụ thể là, sau khi đưa thuốc vào cơ thể một phần lượng thuốc sẽ bị chuyển hóa tại gan hoặc bị thải trừ ở thận, chỉ có một lượng nhỏ thuốc đến tiêu diệt tế bào ung thư và phần còn lại phân bố vào các cơ quan khác của cơ thể làm hại cho tế bào lành, gây cho người bệnh những tác dụng phụ buồn nôn, suy tủy, rụng tóc…Trong mười năm gần đây, nhiều nghiên cứu về vật liệu nano ứng dụng trong lĩnh vực y sinh đang phát triển mạnh mẽ với mong muốn tìm những hệ dẫn truyền thuốc thông minh có thể mang thuốc đến đúng tế bào bệnh và giải phóng đúng mục tiêu, làm giảm thiệt hại cho các bệnh nhân trong điều trị ung thư, thu hút sự chú ý của nhiều nhà khoa học trên khắp thế giới.
Có rất nhiều vật liệu nano đã và đang được nghiên cứu, trong số đó nano silica nổi bật bởi những đặc tính như tính tương thích sinh học cao, khả năng phân hủy sinh học vượt trội, dễ đào thải, dễ tổng hợp, dễ biến tính, kích thước và cấu trúc ổn định, diện tích bề mặt và thể tích lỗ xốp lớn[1, 2]. Tuy nhiên, chính vì thể tích lỗ xốp lớn, thuốc dễ mang vào thì cũng dễ dàng rò rỉ ra trong quá trình mang thuốc lưu thông trong hệ tuần hoàn, như thế sẽ không đạt được mong muốn là dẫn truyền thuốc đúng mục tiêu là tế bào bệnh. Do đó, cầnbiến tính bề mặt hạt nano silica bởi các polymer thiên nhiên với mong muốn tăng hiệu suất mang thuốc, duy trì thời gian mang thuốc và giải phóng đến đúng mục tiêu. Trên cơ sở đó đưa ra đề tài “Nghiên cứu biến tính bề mặt nano silica làm chất mang thuốc chống ung thư” với hi vọng tìm ra một hệ mang thuốc chống ung thư hiệu quả hơn.