- Dung dịch chuẩn Asen 1000 ppm.
- Thuốc thử Bạc đietylđithiocacbamat.
- Methalnol - CH3OH.
-Mẫu cá chuẩn Dogfish Liver Certified Reference Material for Trace Metals (DOLT-3) có hàm lượng Asen tổng số: 10,2 0,5(mg/kg)
2.1.3. Chuẩn bị hóa chất và dung dịch chuẩn.
+ Dung dịch chuẩn asen 10 mg/l
Lấy 1ml dung dịch chuẩn gốc asen 1000 mg/l cho vào bình 100ml định mức đến vạch bằng nước cất hai lần.
+ Dung dịch chuẩn Asen 100 g/l:
Lấy chính xác 1ml dung dịch chuẩn làm việc 10ppm cho vào bình 100ml định mức đến vạch bằng nước cất hai lần.
+ Dung dịch Axit dimetylasinic-DMA mg/l: Cân 28,57mg ( CH3)2AsNaO2.3H2O thêm nước cất, định mức đến 100ml.
+ HNO3 : HClO4 (1: 1): Trộn 100ml HNO3 ? với 100ml HClO4 72%.
+ MeOH : H2O (1 : 1): Trộn 150ml MeOH với 150ml nước cất
hai lần.
+ Axit HCl 15%:
Hút 101,2 ml HCl 37% cho vào định mức đến 250 ml bằng nước cất được 250ml dung dịch HCl 15%.
+ Thuốc thử Bạc đietylđithiocacbamat:
Pha loãng 1ml Mocfolin trong 70ml Clorofom thêm 0,3 g Bạc đietylđithiocacbamat, lắc nhẹ cho đến khi Bạc đietylđithiocacbamat tan hoàn toàn, sau đó định mức đến vạch bằng Clorofom. Dung dịch pha được có màu vàng, được bảo quản trong điều kiện không tiếp xúc với ánh sáng.
+Pha natri bo hiđrua (NaBH4):
Hòa tan 0,4 gam NaOH trong 400ml nước, sau đó thêm 4gam Natri bo hiđrua (NaBH4) vào dung dịch trên, lắc nhẹ cho NaBH4 tan hoàn toàn (dung dịch này chuẩn bị hàng ngày).
+Axit clohiđric HCl 2M:
Pha loãng 165ml Axit clohiđric đặc đến thể tích V = 1 lit bằng nước cất hai lần.
+ Dung dịch Chì axetat:
Hòa tan 10 gam (CH3COO)2Pb.2H2O trong 100ml nước cất hai lần.
2.2. Phương pháp nghiên cứu:
2.2.1.Phương pháp xác định asen :
Phương pháp quang phổ hấp thụ nguyên tử với kỹ thuật hydrua là một trong những phương pháp phổ biến nhất được sử dụng để phân tích asen, do giá thành thiết bị cao, cùng với quy trình vận hành phức tạp, nên chỉ có ít phòng thí nghiệm ở Việt Nam sử dụng phương pháp này để xác định asen. Vì vậy, trong nghiên cứu này, chúng tôi xác định hàm lượng asen trong các mẫu hải sản bằng phương pháp trắc quang.
Nguyên tắc của phương pháp được tóm tắt như sau: Các dạng asen vô cơ hòa tan trong dung dịch, có thể ở dạng As (III) hoặc As (V) được khử về dạng As(III) bằng dung dịch KI vì hiệu suất tạo hydrua của As(V) thấp hơn nhiều so với As(III). Dạng asen này sẽ phản ứng với hidro mới sinh tạo thành khí (AsH3) bởi NaBH4 hoặc kẽm hạt trong môi trường axit (pH=1). Khí Asin giải phóng được hấp thụ trong dung dịch bạc đietylđithiocarbamat, tạo thành hợp chất màu đỏ tím có cực đại hấp thụ tại bước sóng 520 nm.
AsO43-+ 2I- + 2H+ AsO33- + I2+ H2O
3Zn + As3+ + 3H+ 3Zn2+ + AsH3
AsH3+6AgSCSN(C2H5)2 6Ag +3(C2H5)2SCSNH + [(C2H5)2SCSN]As.
Sơ đồ của: Hệ tạo hợp chất mầu của Asin và Bạc đietylđithiocarbamatnhư sau.
Hình 2.1 Hệ tạo hợp chất mầu của Asin và Bạc đietylđithiocarbamat
- Phân tích asen tổng số: Để phân tích hàm lượng tổng asen trong hải sản, mẫu được vô cơ hóa bằng hỗn hợp các axit để chuyển tất cả các dạng asen về asen (V), sau đó asen (V) được khử về asen (III) bằng KI và xác định bằng phương pháp đo quang.
- Phân tích các dạng asen vô cơ: Mẫu hải sản được chiết trong hỗn hợp methanol- nước bằng siêu âm, sau đó ly tâm và xác định hàm lượng tổng asen vô cơ trong dịch chiết bằng phương pháp đo quang.
- Phân tích các dạng asen hữu cơ: Hàm lượng asen hữu cơ được tính toán dựa trên hàm lượng asen tổng số và hàm lượng asen vô cơ
2.2.2. Phương pháp xử lý mẫu:
- Phân tích asen tổng số:
Trong mẫu hải sản, asen được liên kết chặt chẽ với các protein. Do đó trước khi định lượng, cần phá vỡ nền protein của mẫu để đưa các dạng asen về dạng vô cơ bằng một phương pháp vô cơ hóa thích hợp. Trong nghiên cứu này, chúng tôi sử dụng kỹ thuật vô cơ hóa ướt có sử dụng hỗn hợp các axit HNO3, HClO4 và H2SO4 theo các tỷ lệ thích hợp.
- Phân tích asen vô cơ:
Để phân tích hàm lượng tổng asen vô cơ trong các mẫu hải sản, chúng tôi sử dụng quy trình chiết của Nguyễn Đình Thuất[13], mẫu được chiết với MeOH-H2O bằng siêu âm, sau đó ly tâm và tiến hành phân tích bằng phương pháp trắc quang.
2.3. Đối tượng nghiên cứu:
Asen là nguyên tố độc hại, có khả năng tích lũy sinh học cao, đặc biệt là trong các đối tượng thủy hải sản, tuy nhiên mức độ độc hại của asen lại phụ thuộc vào dạng hóa học của chúng. Do vậy đối tượng nghiên cứu của luận văn này là sự tích lũy và phân bố các dạng asen vô cơ và hữu cơ trong các loại hải sản bao gồm: Tôm, cá ngừ, cá thu, cá khoai, cá ngân, sao biển, vẹm xanh, ngao..
2.4. Nội dung nghiên cứu.
Chúng tôi tiến hành nghiên cứu xác định hàm lượng Asen tổng số, dạng hợp chất Asen vô cơ, dạng hợp chất Asen hữu cơ trong các mẫu hải sản trên với nội dung như sau:
2.4.1. Nghiên cứu các điều kiện tối ưu để xác định asen bằng phương pháp đo quang:
- Khảo sát sự hình thành hợp chất mầu của asin với thuốc thử
- Khảo sát cực đại hấp thụ của hợp chất màu.
- Khảo sát thời gian phản ứng.
- Khảo sát ảnh hưởng của thể tích mẫu, thể tích thuốc thử.
- Xây dựng đường chuẩn để xác định Asen.
2.4.2. Xây dựng qui trình phân tích cho các đối tượng mẫu nghiên cứu.
- Nghiên cứu, khảo sát và lựa chọn phương pháp xử lý mẫu thích hợp để định lượng Asen.
- Nghiên cứu, khảo sát ảnh hưởng của các loại axit và nồng độ axit đến qui trình xử lý mẫu.
- Xác định qui trình phân tích Asen tổng số, qui trình phân tích dạng Asen hữu cơ và vô cơ trong các mẫu hải sản.
- Phân tích định lượng Asen tổng số, xác định hàm lượng các dạng Asen hữu cơ và vô cơ trong các mẫu hải sản theo qui trình đã xây dựng và xác định được.
- Xử lý và đánh giá kết quả thực nghiệm.
- Kết luận về tính độc của các hải sản đã phân tích.
2.5. Lấy mẫu và bảo quản mẫu.
- Các mẫu cá, tôm sú, vẹm xanh, sao biển, ngao trước khi phân tích được rửa sạch bằng nước cất hai lần, cất vào tủ đông cho đến khi đông đá hoàn toàn, sau đó, mẫu được làm khô bằng phương pháp đông khô chân không để không phá vỡ cấu trúc ban đầu của mẫu, giữ nguyên được dạng hữu cơ trong mẫu. Cuối cùng, nghiền nhỏ mẫu và bảo quản ở nhiệt độ -50C.
Mẫu hải sản
Mẫu đã vô cơ hóa
Mẫu chiết (dạng dung dịch)
Mẫu hải sản dạng bột
Asen tổng số
Dạng Asen vô cơ
Dạng Asen hữu cơ
Hình 2.1: Quy trình xác định tổng số, tổng dạng Asen trong một số hải sản bằng phương pháp trắc quang
CHƯƠNG III
KẾT QUẢ VÀ THẢO LUẬN
3.1. Khảo sát các điều kiện tối ưu cho quá trình tạo hợp chất màu
Để nghiên cứu sự tạo thành hợp chất màu của bạc Đietylđithiocacbamat với khí Asin- AsH3 bằng phương pháp trắc quang, trước hết phải biết được phổ hấp thụ của thuốc thử và của phức. Vì vậy, công việc đầu tiên là khảo sát phổ của chúng.
3.1.1. Khảo sát phổ hấp thụ của thuốc thử:
Dùng pipet lấy chính xác 10ml dung dịch HCl 15% vào bình phản ứng, thêm 4g Zn, đồng thời lắp bình hấp thụ của hệ tạo phức đã có sẵn 4ml dung dịch bạc Đietylđithiocacbamat vào bình phản ứng, khuấy từ ở bình phản ứng trong thời gian 20 phút, để yên 10 phút.. Sau đó đem đo mật độ quang của dung dịch thuốc thử với cuvet 1cm ở dải sóng 350nm-750nm. Dung dịch so sánh là Clorofom.
Kết quả đo được biểu diễn trên hình 3.1.
3.1.2. Khảo sát phổ hấp thụ của hợp chất màu
- Lấy 50 ml dung dịch Asen(III) 50 g/l vào bình phản ứng của hệ tạohợp chất màu, thêm 1ml dung dịch KI 10%, 10ml dung dịch HCl 15% , và 4g Zn, đồng thời lắp bình hấp thụ của hệ tạo phức đã có sẵn 4ml dung dịch bạc Đietylđithiocacbamat vào bình phản ứng. Khuấy từ ở bình phản ứng trong thời gian 20 phút. Dạng asen này phản ứng với hidro mới sinh tạo thành khí (AsH3) trong môi trường axit (pH=1). Khí Asin giải phóng được hấp thụ trong dung dịch bạc đietylđithiocarbamat tạo hợp chất màu, sau đó, lấy phần hợp chất màu vừa tạo được đem đo phổ ở dải sóng 350nm - 750nm, với dung dịch so sánh là Clorofom, ta thu được phổ hấp thụ của hợp chất màu nghiên cứu ở hình 3.1.
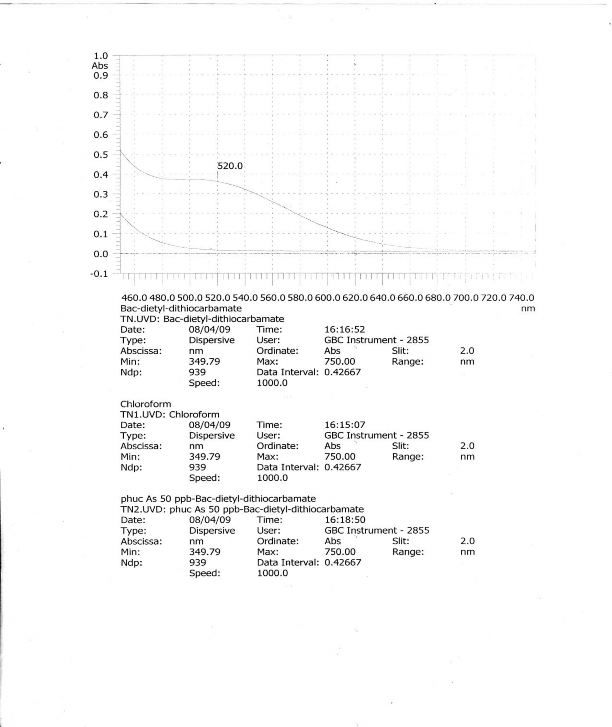
Hình 3.1. Phổ hấp thụ của thuốc thử và phổ hấp thụ của hợp chất màu của Asen
- Dựa vào phổ hấp thụ của thuốc thử và phổ hấp thụ của phức màu của Asen cho thấy hợp chất màu có đỉnh hấp thụ đạt cực đại tại bước sóng λ max= 520nm. Cũng tại bước sóng này thuốc thử Bạc đietylđithiocacbamat và dung
dịch clorofomkhông có đỉnh hấp thụ, vì vậy, để đảm bảo độ chính xác và độ
nhạy của phép phân tích, chúng tôi chọn bước sóng λ = 520nm, khi khảo sát mật độ quang trong các phép đo về sau.
Dung dịch so sánh được sử dụng trong các phép đo là Clorofom vì tuy thuốc thử Bạc đietylđithiocacbamat có màu, song vì thuốc thử Bạc đietylđithiocacbamat và dung dịch clorofom đều không có đỉnh hấp thụ tại bước sóng 520nm. Vì thế, trong các phép đo về sau chúng tôi sử dụng dung dịch so sánh là clorofom.
3.1.3. Khảo sát thời gian tối ưu cho việc tạo hợp chất màu.
Để xét đến khoảng thời gian nào thì phức có độ quang ổn định, chúng tôi tiến hành khảo sát ảnh hưởng của thời gian tới sự tạo hợp chất màu như sau:
- Lấy 50 ml dung dịch Asen(III) 50 g/l vào bình phản ứng của hệ tạo Asin, thêm 1ml dung dịch KI 10%, 10ml dung dịch HCl 15% , và 4g Zn, đồng thời lắp bình hấp thụ đã có sẵn 4ml dung dịch bạc Đietylđithiocacbamat vào bình phản ứng. Khuấy từ ở bình phản ứng với thời gian thay đổi như trong bảng 3.1 tạo ra hơi Asin, hơi Asin giải phóng ra được dẫn vào bình hấp thụ của hệ tạo phức và phản ứng với 4ml dung dịch thuốc thử Bạc đietylđithiocacbmat trong bình hấp thụ tạo hợp chất màu, tiếp theo, đo mật độ quang của hợp chất màu thu được ở các thời gian trên tại bước sóng 520nm với dung dịch so sánh là clorofom, kết quả thu được trong bảng 3.1 và được biểu diễn trên hình 3.2.
Bảng 3.1: Sự phụ thuộc của mật độ quang vào thời gian
Mật độ quang(A) | |
0 | 0,001 |
5 | 0,112 |
10 | 0,160 |
Có thể bạn quan tâm!
-
 Các Dạng Asen Trong Môi Trường Biển :
Các Dạng Asen Trong Môi Trường Biển : -
 Các Phương Pháp Tách Chiết Và Bảo Quản Mẫu Trong Phân Tích Các Dạng Asen.
Các Phương Pháp Tách Chiết Và Bảo Quản Mẫu Trong Phân Tích Các Dạng Asen. -
 Ổn Định Và Duy Trì Những Dạng Ban Đầu Của Mẫu.
Ổn Định Và Duy Trì Những Dạng Ban Đầu Của Mẫu. -
 Ảnh Hưởng Của Ph Đến Quá Trình Khử Asen(Iii) Thành Asin
Ảnh Hưởng Của Ph Đến Quá Trình Khử Asen(Iii) Thành Asin -
 Sự Phụ Thuộc Giữa Độ Hấp Thụ Vào Nồng Độ Asen
Sự Phụ Thuộc Giữa Độ Hấp Thụ Vào Nồng Độ Asen -
 Kết Quả Phân Tích Asen Tổng Số Trong Mẫu Hải Sản
Kết Quả Phân Tích Asen Tổng Số Trong Mẫu Hải Sản