silicagen với hệ dung môi n-hexan:clorofom thu được chất ĐC-1, chất này cho các phản ứng định tính của terpenoit.
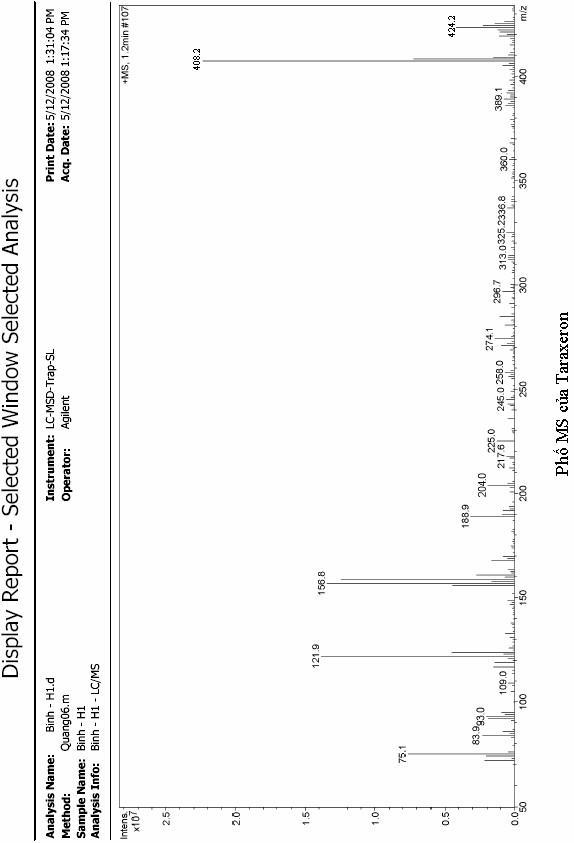
Khối lượng phân tử của chất ĐC-1 được xác định bằng phổ khối LC- MS cho biết khối lượng phân tử của [M+] m/z bằng 424,2 tương ứng với khối lượng phân tử bằng 424 u và tương ứng với công thức phân tử C30H48O.
Trong phổ LC-MS còn xuất hiện pic m/z 408,2 điều này tương ứng với
mảnh [M-O]+ với m/z bằng 408
Phổ FT-IR: cho thấy các vân hấp thụ của nhóm xeton (C=O) ở νmax = 1720cm-1, liên kết đôi (C=C) ở νmax = 1500cm-1, các nhóm CH3 ở νmax = 3050cm-1 và các nhóm CH ở νmax = 2940cm-1, không phát hiện thấy các vân hấp thụ của nhóm OH. Điều này có thể khẳng định được hợp chất ĐC-1
không có chức rượu mà là có chức xeton.
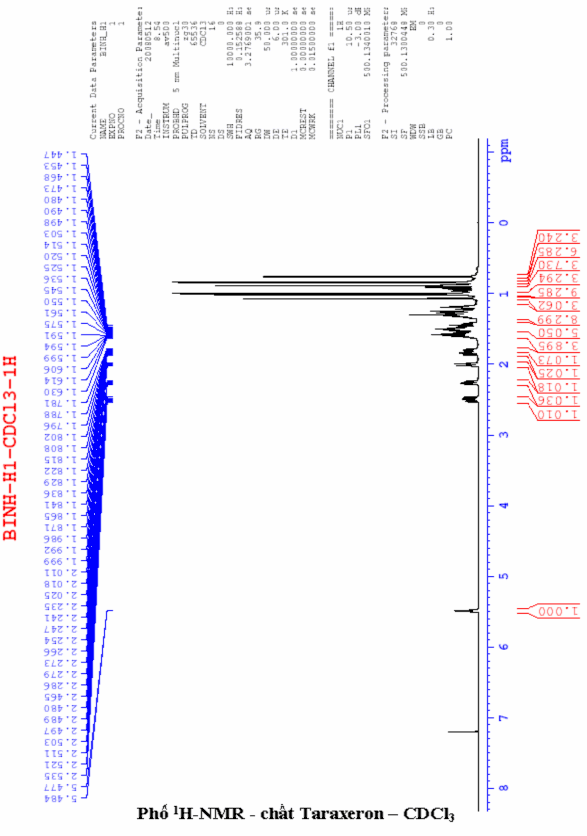
Phổ 1H-NMR và phổ DEPT: cho biết hợp chất ĐC-1 có tín hiệu của 8 nhóm CH3 đều ở dạng singlet (xem hình 3.2 và 3.4) có các độ chuyển dịch hoá học như sau: ở độ chuyển dịch δ = 0,762ppm (3H, s, CH3); δ = 0,841ppm (3H, s, CH3); δ = 0,847ppm (3H, s, CH3); δ = 0,885ppm (3H, s, CH3); δ = 0,996ppm (3H, s, CH3); δ = 1,011ppm (3H, s, CH3); δ = 1,021ppm (3H, s,
CH3); δ = 1,07ppm (3H, s, CH3). Độ dịch chuyển hoá học ở δ = 5,48ppm
(1H, d, J = 3,21 và 8,17Hz) là của proton liên kết tại cacbon ở liên kết đôi (nhóm = CH tại C15).
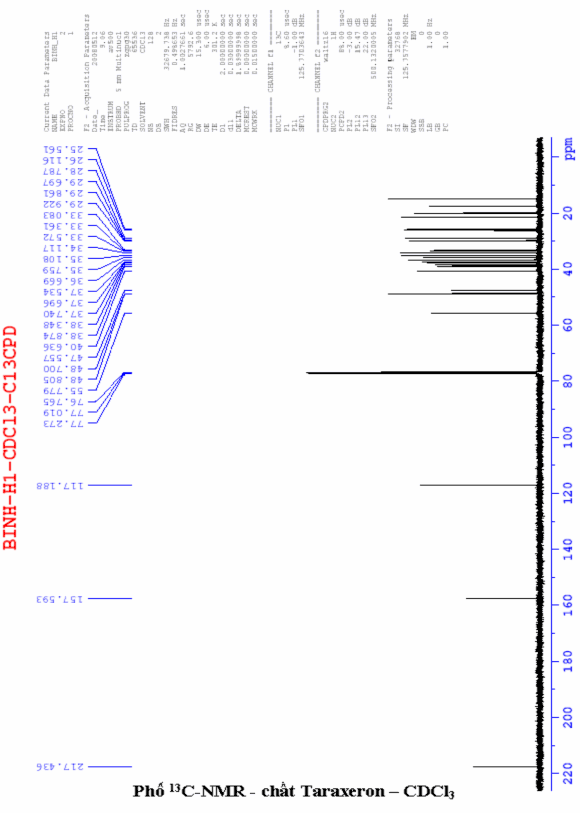
Phổ 13C-NMR: nhận thấy nguyên tử cacbon ở trạng thái lai hoá sp2
thuộc nhóm =CH có độ chuyển dịch hoá học δ = 117,19ppm. Nguyên tử cacbon bậc 4 cũng ở trạng thái lai hoá sp2tham gia vào liên kết đôi với nguyên tử này có độ chuyển dịch hoá học ở δ = 157,59ppm.
Phổ 13C-NMR còn cho một tín hiệu ở trường rất yếu tương ứng với độ chuyển dịch hoá học δ = 217,43ppm đặc trưng cho cacbon trong nhóm cacbonyl tại vị trí C-3.
Như vậy, phổ NMR hoàn toàn phù hợp với phổ FT-IR không thấy có vân đặc trưng của nhóm OH mà lại thấy xuất hiện vân đặc trưng của C=O. Các nguyên tử H đối với nhóm C=O thấy chỉ có 2H với δ = 2,50ppm (2H, dd, J = 7,1 và 11Hz), còn có 2 proton ở vị trí của nhóm =CH (tại C16) có độ chuyển dịch hoá học δ = 2,27ppm (2H, dd, J = 3,3 và 4,08 và 6,39).
Trên cơ sở phân tích các tính chất hoá học, nhất là phân tích các thông tin có được từ phổ LC- MS, FT-IR, phổ cộng hưởng từ hạt nhân 1H-NMR, 13C-NMR, phổ DEPT, phổ HMBC, HSQC, phổ H-H COSY và phần mềm
ACD/HNMR ACD/CNMR mô phỏng phổ NMR cũng đã cho phép chúng tôi quy kết hợp chất ĐC-1 là một triterpen phải có công thức cấu tạo như sau:
29 30
11 12
1 24 9 27
23 19 20 21
18 22
13 17
28
2 10
16
8 14
15
3 4 5 7
O6
25 26
Taraxeron (hay Frendoolean-14-en-3-on)
Bảng 3.1. Phổ 13C-NMR và 1H-NMR của taraxeron (ĐC-1) từ lá đỏ ngọn
13C-NMR (δ-ppm) | ACD/13C- NMR (δ-ppm) | 1H-NMR (δ-ppm) | |
1 | 38,35 | 38,4 | Vùng (1,2 - 1,6) |
2 | 33,08 | 34,1 | 2,5 (2H; dd; 7,1 và 11,0) |
3 | 217,3 | 217,3 | - |
4 | 47,56 | 47,6 | - |
5 | 55,77 | 55,8 | (1,99) |
6 | 19,91 | 20,0 | Vùng (1,2 - 1,6) |
7 | 33,57 | 35,2 | Vùng (1,2 - 1,6) |
8 | 38,87 | 38,9 | - |
9 | 48,8 | 48,7 | (1,78 - 1,87) |
10 | 33,57 | 37,6 | - |
11 | 17,44 | 17,5 | Vùng (1,2 - 1,6) |
12 | 36,67 | 35,8 | Vùng (1,2 - 1,6) |
13 | 37,74 | 37,7 | - |
14 | 157,59 | 157,6 | - |
15 | 117,19 | 117,2 | 5,48 (1H; d; 3,21; 8,17) |
16 | 34,12 | 36,7 | 2,27 (2H; dd; 3,3; 4;1; 6,4) |
17 | 35,57 | 37,7 | - |
18 | 48,7 | 48,8 | (1,78 - 1,87) |
19 | 40,64 | 40,7 | Vùng (1,2 - 1,6) |
20 | 28,79 | 28,8 | - |
21 | 35,11 | 33,6 | Vùng (1,2 - 1,6) |
22 | 37,69 | 33,1 | Vùng (1,2 - 1,6) |
23 | 29,92 | 29,9 | 0,76 - 1,07 (24H của 8 nhóm CH3) |
24 | 14,79 | 14,8 | |
25 | 29,86 | 29,9 | |
26 | 21,34 | 21,5 | |
27 | 25,56 | 25,6 | |
28 | 26,12 | 26,2 | |
29 | 33,36 | 33,4 | |
30 | 21,47 | 21,4 |
Có thể bạn quan tâm!
-
 Nghiên cứu hoá học và nhận dạng một số nhóm chất có trong cây đỏ ngọn (cratoxylum prunifolium kurtz) - 2
Nghiên cứu hoá học và nhận dạng một số nhóm chất có trong cây đỏ ngọn (cratoxylum prunifolium kurtz) - 2 -
 Những Nghiên Cứu Hoá Thực Vật Loài Cratoxylum Prunifolium.
Những Nghiên Cứu Hoá Thực Vật Loài Cratoxylum Prunifolium. -
 Kết Quả Thử Hoạt Tính Sinh Học Của Dịch Chiết Thô
Kết Quả Thử Hoạt Tính Sinh Học Của Dịch Chiết Thô -
![Phổ 13 C-Nmr Của Các Chất Đc-2 Và Stingmasterol [16]](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Phổ 13 C-Nmr Của Các Chất Đc-2 Và Stingmasterol [16]
Phổ 13 C-Nmr Của Các Chất Đc-2 Và Stingmasterol [16] -
 Số Liệu Phổ Nmr Của Đe-1 Và Số Liệu Phổ Nmr Trong
Số Liệu Phổ Nmr Của Đe-1 Và Số Liệu Phổ Nmr Trong -
 Phổ 13 C-Nmr Của Chất Axit Gallic
Phổ 13 C-Nmr Của Chất Axit Gallic
Xem toàn bộ 118 trang tài liệu này.
Hình 3.1
Hình 3.2
Hình 3.3

Hình 3.4
3.3.2. Stingmast -5,22-dien-24R-3β-ol (ĐC-2)
Chất ĐC-2 là chất rắn kết tinh, có nhiệt độ nóng chảy ở 1520-1550C, tách được từ dịch chiết clorofom, phân lập bằng sắc kí cột silicagen, rửa giải bằng hệ dung môi n-hexan-clorofom (90:10).
Phổ EI-MS cho pic ion phân tử [M+] ở 412 m/z. Các phổ FT-IR, 1H-
NMR và 13C-NMR đều khẳng định sự có mặt của nhóm hydroxyl, phổ FT- IR có vân 3410cm-1 rộng, còn ở phổ NMR cho δH-3α = 3,47ppm và δC-3 = 71,6ppm). Phân tử có hai nối đôi không liên hợp (IR cho νmax ở 1622cm-1).
Phổ 1H-NMR của các proton thuộc nhóm metyl (CH) cũng đã khẳng
định điều ấy, δH-6 = 5,33ppm (1H, dd, j =15Hz và 2Hz); δH-22 = 5,15ppm (1H, dd, j =15Hz và 5Hz); δH-23 = 5,01ppm (1H, dd, j =15Hz và 5Hz). Phổ 13C- NMR cho thấy δC-5 = 139,2ppm; δC-6 = 121,4ppm; CC-22 = 138,4ppm và δC-23
= 129,2ppm. So sánh các số liệu phổ 1H-NMR và 13C-NMR của chất ĐC-2
với số liệu phổ NMR của stingmasterol [16] hoàn toàn tương tự nhau và được chỉ ra ở bảng 3.2.
Dựa trên phân tích các số liệu về phổ EI-MS, FT-IR và các phổ NMR của hợp chất ĐC-2 hoàn toàn phù hợp với cấu trúc của chất Stingmast -5,22-dien- 24R-3β-ol.
29
28
21 27
22 24
19 20
12 17
23 25
26
2
HO 3
18 11
1
9
10
5
4 6
13 16
14 15
8
7
Stingmast -5,22-dien-24R-3β-ol




![Phổ 13 C-Nmr Của Các Chất Đc-2 Và Stingmasterol [16]](https://tailieuthamkhao.com/uploads/2022/05/15/nghien-cuu-hoa-hoc-va-nhan-dang-mot-so-nhom-chat-co-trong-cay-do-ngon-6-1-120x90.jpg)

