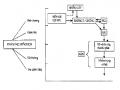
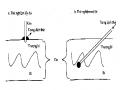
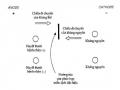
Trong bệnh thiếu máu ác tính có xuất hiện một tự kháng thể ngăn cản sự hấp thụ vitamine B12 theo đường ăn uống. Chúng ta biết rằng B12 không thể hấp thu dưới dạng tự do được, mà cần phải được gắn vào một protein do dạ dày tiết ra gọi là yếu tố nội, và chỉ có phức hợp B12 - yếu tố nội mới có thể hấp thụ qua niêm mạc ruột. Trong bệnh nhân thiếu máu ác tính người ta đã tìm thấy một kháng thể có khả năng phong bế tác dụng của yếu tố nội. Kháng thể này được tiết ra bởi các tương bào có mặt trong niêm mạc dạ dày và phong bế yếu tố nội dẫn đến ngăn cản hấp thu B12 và bệnh thiếu máu ác tính hình thành (Hình 11.4).
Bình thường
Thiếu máu ác tính
Thức ăn
Tếbào thành dạ dày
Thức ăn
B12 được hấp thu từ lòng ruột
B12 được hấp thu từ lòng ruột
Hình 11.4. Mất hấp thu vitamin B12 trong bệnh thiếu máu ác tính Bình thường vitamin B12 được hấp thu qua niêm
mạc ruột dưới dạng
một phức hợp với yếu tố nội (IF). Trong bệnh thiếu máu ác tính tự kháng thể chống yếu tố nội trong dịch dạ dày đã kết hợp với yếu tố nội làm cho
Các ví dụ khác về nguyên nhân gây bệnh của tự kháng thể là trường hợp hội chứng Goodpasture, kháng thể kháng màng đáy cầu thận. Trong SLE, sự lắng đọng của phức hợp kháng nguyên - kháng thể tại cầu thận là nguyên nhân của tổn thương thận; mà trong thành phần của phức hợp có rất nhiều loại tự kháng thể tham gia; kháng thể kháng nhân, kháng thể kháng DNA, kháng thể kháng cardiolipin,.v.v.
Tóm lại, chúng ta có thể xem phản ứng tự miễn đóng vai trò chủ yếu trong nguyên nhân của hầu hết các bệnh tự miễn.
11.6. Cơ chế bệnh sinh
Cho đến nay, người ta đã hoàn toàn công nhận rằng có tồn tại trong cơ thể các tế bào lymphô tự phản ứng. Còn các tự kháng nguyên phản ứng với các tế bào này như thyroglobulin chẳng hạn, trước đây được coi như ẩn núp trong tuyến giáp không tiếp xúc với hệ miễn dịch thì đến nay được biết là cũng có mặt trong hệ tuần hoàn cùng với các lymphô. Do đó tự kháng nguyên lẫn tế bào lymphô tự phản ứng đều có điều kiện tiếp xúc với nhau ở
người bình thường. Điều này có nghĩa rằng, ở người bình thường đã có một cơ chế ngăn cản phản ứng tự miễn. Và tế bào T ức chế được xem như có vai trò quan trọng trong việc ức chế tính tự phản này. Hình 11.5 mô tả một cơ chế mà trong đó sự kiểm soát bình thường đối với tính tự miễn bỏ qua, người ta gọi đó là cơ chế đường tắt (bypass). Hoạt động kiểm soát bình thường trong cơ thể được đảm trách bởi nhiều loại tế bào ức chế tạo nên một phức hợp ức chế do tế bào T phụ trách. Tuy nhiên, khi có sai sót xảy ra cho tế bào T ức chế thì phản ứng tự miễn có thể xuất hiện.
Điều thú vị là trên lâm sàng người ta đã tìm thấy những người có quan hệ họ hàng với bệnh nhân SLE có sai sót ở các tế bào T ức chế. Điều này nói lên rằng: một là, sự sai sót ở tế bào T ức chế không phải là hậu quả của bệnh, và hai là, tình trạng sai sót này không thể tự nó gây ra bệnh SLE. Điều này cùng với những điều đã đề cập trên đây chứng tỏ rằng có nhiều yếu tố đã tham gia gây bệnh tự miễn. Đồng thời,cũng từ đó, có thể suy thêm ra rằng, những bất thường của tế bào T điều hòa đặc hiệu kháng nguyên hoặc đặc hiệu idioptyp cũng đã tham gia vào cơ chế gây nên.
Trên một số thí nghiệm người ta phát hiện rằng một số phân tử thụ thể trên bề mặt tế bào bình thường có tính chất “im lặng” miễn dịch vì màng những tế bào này không có kháng nguyên MHC lớp II; nhưng khi được kích thích một cách thích hợp thì có thể xuất hiện sản phẩm MHC lớp II. Ví dụ tế bào tuyến giáp có thể tạo phân tử HLA-D khi được kích thích bằng các lectin thực vật và các phân tử này cùng với các thụ thể bề mặt đã kích thích các tế bào T tự phản ứng tạo ra phản ứng tự miễn đối với thụ thể tế bào tuyến giáp.
Người ta cũng đã đưa ra nhiều cơ chế khác về sự hình thành bệnh tự miễn. Các cơ chế đó được minh họa ở các hình 11.6, 11.7, và 11.8.
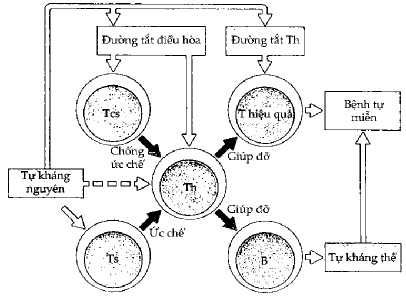
Hình 11.5. Bệnh tự miễn do mất kiểm soát phản ứng tự miễn
Tế bào B tự phản ứng, tế bào T hiệu quả và tự kháng nguyên bình thường vẫn có mặt trong cơ thể nhưng không được khởi động nhờ sự ức chế của tế bào Ts đối với tế bào Th tương ứng. Khi có một nguyên nhân gí đó hoạt hóa tế bào Th này hoặc có tế bào chống Ts (Tcs) xuất hiện thì phản ứng tự miễn không còn bị kiểm soát nữa và bệnh tự miễn xảy ra.
Đặc biệt, Hình 11.7 minh họa một ví dụ thú vị là mạng idioptyp có thể tham gia gây bệnh tự miễn bằng cách tác động vào tế bào T hoặc tế bào B tự phản ứng có mang idioptyp chung phản ứng chéo với idioptyp trên một kháng thể được tạo thành do kích thích của vi sinh vật hoặc phản ứng chéo với cấu trúc kháng nguyên trên vi sinh vật. Nhưng, ngay cả trong trường hợp này, phản ứng tự miễn cũng vẫn không xảy ra nếu không có sai sót ở mức tế bào T ức chế và điều này lại một lần nữa nhấn mạnh vai trò đa yếu tố trong việc thiết lập một phản ứng tự miễn kéo dài.
11.7. Chẩn đoán và tiên lượng
Dù cho quan hệ giữa kháng thể và quá trình bệnh có thế nào đi nữa, thì sự hiện diện của kháng thể rò ràng là đã cung cấp những dấu hiệu có giá trị để chẩn đoán bệnh. Một ví dụ điển hình là người ta đã tìm kháng thể kháng ty lạp thể để chẩn đoán xác định xơ gan mật tiên phát. Điều này giúp cho các nhà lâm sàng khỏi phải mở bụng thăm dò như thời kỳ trước đây có thể gây nhiều nguy hiểm cho bệnh nhân.
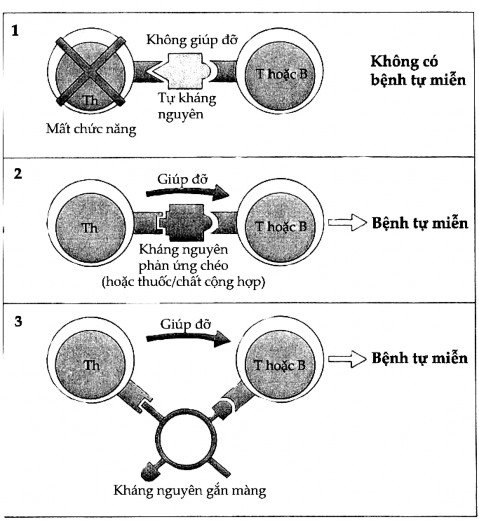
Hình 11.6. Khởi động phản ứng tự miễn qua đường tắt 1 đối với tế bào T
(1) Bình thường phản ứng tự miễn không xảy ra vì tế bào T tự phản ứng và tự kháng nguyên bị ức chế hoặc loại bỏ. (2) Khi có kháng nguyên phản ứng chéo xuất hiện, một quần thể Th mới sẽ tạo ra phản ứng giúp đỡ. (3) Cũng có khi một phân tử màng lại có tác dụng như tự kháng nguyên để tạo hiệu ứng giúp đỡ tạo ra bệnh tự miễn.
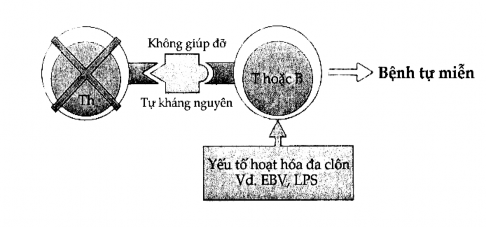
Hình 11.7. Khởi động phản ứng tự miễn bằng đường tắt 2 đối với tế bào T
Các tế bào tự phản ứng có thể được kích thích bởi các chất hoạt hóa đa clôn như virus Epstein-Barr hoặc lipopolysaccharid vi khuẩn.
Tự kháng thể cón có giá trị tiên lượng. Ví dụ trường hợp một đứa trẻ có anh chị em mắc bệnh đái đường phụ thuộc insulin, nó có chung HLA với anh chị, đồng thời trong huyết thanh có cả khảng thể khảng tế bào đảo tụy. Sau 3 năm nghiên cứu, thì thấy ở đứa trẻ cũng xuất hiện bệnh đái tháo đường nặng, điều này chứng tỏ giá trị tiên lượng của các tự kháng thể này, và kháng thể đã xuất hiện khá lâu trước khi bệnh xuất hiện.
11.8. Điều trị
Một cách kinh điển, trong các bệnh tự miễn đặc hiệu cơ quan, tổn thương thường điều chỉnh được nhờ kiểm soát chuyển hóa. Ví dụ, trong suy giáp, thiếu hormon tuyến giáp có thể khống chế được bằng cách cho thyronxin còn nhiễm độc giáp thì thuốc kháng giáp thường có thể cho tác dụng tốt. Trong thiếu máu ác tính, điều chỉnh chuyển hóa có thể thực hiện được bằng cách cho tiêm vitamin B12 bổ sung, và trong nhược cơ năng thì dùng các chất ức chế cholinesterase. Nếu chức năng tuyến hoàn toàn mất và không thể bù được bằng hormon như trong trường hợp viêm thận lupus hoặc viêm khớp dạng thấp mạn tính thì cần phải tiến hành ghép mô hoăc thay cơ quan giả.
Th (kháng id)
T hoặc B
Hình 11.8. Khởi động phản ứng tự miễn bằng con đường idiotyp
Phản ứng tự miễn cũng có thể xảy ra nếu tế bào T hoặc B tự phản ứng mang một idiotyp phổ biến có phản ứng chéo với idiotyp trên kháng thể hoặc với cấu trúc trên vi khuẩn.
Các liệu pháp ức chế miễn dịch kinh điển dùng thuốc chống phân bào có thể dùng để giảm phản ứng miễn dịch nhưng do những phản ứng phụ của thuốc mà các thuốc này chỉ dùng trong trường hợp bệnh quá nặng như SLE, viêm da cơ. Tất nhiên, các thuốc chống viêm có thể dùng cho các bệnh thấp.
Bởi vì chúng ta đã biết quá nhiều về cơ chế bệnh sinh nên tùy theo từng khâu của cơ chế bệnh mà ta có thể dùng những phương tiện khác để khống chế bệnh tự miễn (Hình 11.9). Đặc biệt việc khai thác mạng idioptyp để ức chế các idioptyp trên tế bào T khỏi động và T hiệu quả đang là một hứa hẹn khả quan.
Kháng lớp II Kháng T4 Thuốc
Kháng phân bào
Kiểm soát chuyển hóa
Thuốc Kháng viêm
Hình 11.9. Điều trị bệnh tự miễn
Trên sơ đồ, các phương tiện điều trị kinh điển hiện nay được in bằng chữ thường trên nền xám. Còn các biện pháp mới được in nghiêng đậm.
11.9. Một số hiệu quả thuận lợi của phản ứng tự miễn
Cũng có khi việc gây phản ứng tự miễn cho một cơ thể lại tỏ ra có lợi cho cơ thể đó (Bảng 11.2). Mặc dù đây là những việc làm có thể thực hiện được, vấn đề chính (nhưng không phải là duy nhất) đối với bệnh nhân là làm thế nào để nhận diện chính xác các epitop cần gây phản ứng tự miễn mà không gây phản ứng chéo với các tự kháng nguyên khác; và ngoài ra là chúng ta phải làm thế nào
để tìm được những chất tải (carrier) hiệu quả nhất cũng như các tá chất thích hợp
để có thể gây phản ứng ở mức độ mong muốn.
Bảng 11.2. Các hiệu quả có lợi của phản ứng tự miễn
Nhằm mục đích | |
1. Human chorionic gonadotropin | Chống thụ tinh |
2. LHRH | Giả thiến (đối với bò thịt) |
3. Ung thư | Điều trị bằng miễn dịch |
4. Idioptyp | Điều chỉnh đáp ứng miễn dịch |
Có thể bạn quan tâm!
-
 Hội Chứng Thiếu Hụt Miễn Dịch Mắc Phải (Aids)
Hội Chứng Thiếu Hụt Miễn Dịch Mắc Phải (Aids) -
 Các Phương Pháp Điều Trị Nhằm Ngăn Ngừa Hoặc Loại Trừ Nhiễm Hiv-1. (Rt = Enzym Sao Chép Ngược)
Các Phương Pháp Điều Trị Nhằm Ngăn Ngừa Hoặc Loại Trừ Nhiễm Hiv-1. (Rt = Enzym Sao Chép Ngược) -
 Đáp Ứng Tự Miễn Có Phụ Thuộc Kháng Nguyên Không?
Đáp Ứng Tự Miễn Có Phụ Thuộc Kháng Nguyên Không? -
 Định Lượng Immunoglobulin Và Các Protein Đặc Hiệu Khác
Định Lượng Immunoglobulin Và Các Protein Đặc Hiệu Khác -
 Các Thử Nghiệm Bì. (A) Thử Nghiệm Lẩy; (B) Thử Nghiệm Nội Bì.
Các Thử Nghiệm Bì. (A) Thử Nghiệm Lẩy; (B) Thử Nghiệm Nội Bì. -
 Miễn dịch học Phần 2 - 14
Miễn dịch học Phần 2 - 14