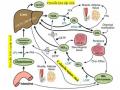
+ Lô trị 2: (uống cao chiết liều thấp): 2/3 mẫu bệnh phẩm gan có thoái hóa nhẹ tế bào gan; 1/3 mẫu bệnh phẩm có thoái hóa vừa tế bào gan.
1
2
3
Lô chứng Lô trị 1 Lô trị 2
Hình 3.3: Nhuộm HE cho các mô gan với độ phóng đại 400x
1. Tế bào gan bình thường. 2. Tế bào gan thoái hóa nhẹ. 3. Tế bào gan thoái hóa vừa.
Hình thái vi thể thận:
2
1
1
2
2
1
Lô chứng Lô trị 1 Lô trị 2
Hình 3.4: Nhuộm HE cho các mô thận với độ phóng đại 400x
1. Cầu thận bình thường. 2. Ống thận bình thường.
Vi cấu trúc gan, thận của chuột cống trắng: với liều 36 mg/kg/ngày, không có tổn thương rõ ràng về vi cấu trúc gan, thận của chuột cống trắng sau 90 ngày dùng thuốc so với lô đối chứng. Liều 108 mg/kg/ngày có tổn thương vi cấu trúc gan mức độ nhẹ và vừa so với nhóm chứng sinh học sau 90 ngày dùng thuốc không có tổn thương vi cấu trúc thận.
3.2. TÁC DỤNG CỦA CAO CHIẾT TỪ LÁ CÂY CHÈ VẰNG (Jasminum subtriplinerve Blume Oleaceae) TRÊN MÔ HÌNH RLLPM THEO CƠ CHẾ NỘI SINH
Bảng 3.4: Ảnh hưởng của lô mô hình P-407 lên chuột nhắt trắng (mmol/L)
Lô chứng sinh học | Lô mô hình P-407 | % thay đổi | |
TG | 1,39 ± 0,31 | 10,76 ± 0,87 *** | ↑ 674,1 % |
TC | 2,55 ± 0,40 | 7,61 ± 0,53 *** | ↑ 198,4 % |
HDL-C | 0,56 ± 0,03 | 0,58 ± 0,04 | ↑ 3,57 % |
non-HDL-C | 2,00 ± 0,39 | 7,03 ± 0,53 *** | ↑ 251,5 % |
Có thể bạn quan tâm!
-
 Đánh giá tính an toàn và tác dụng trên các thông số lipid máu của cao chiết từ lá cây Chè vằng Jasminum subtriplinerve Blume Oleaceae trên thực nghiệm - 1
Đánh giá tính an toàn và tác dụng trên các thông số lipid máu của cao chiết từ lá cây Chè vằng Jasminum subtriplinerve Blume Oleaceae trên thực nghiệm - 1 -
 Đánh giá tính an toàn và tác dụng trên các thông số lipid máu của cao chiết từ lá cây Chè vằng Jasminum subtriplinerve Blume Oleaceae trên thực nghiệm - 2
Đánh giá tính an toàn và tác dụng trên các thông số lipid máu của cao chiết từ lá cây Chè vằng Jasminum subtriplinerve Blume Oleaceae trên thực nghiệm - 2 -
 Giới Thiệu Về Cao Chiết Lá Cây Chè Vằng (Jasminum Subtriplinerve Blume Oleaceae)
Giới Thiệu Về Cao Chiết Lá Cây Chè Vằng (Jasminum Subtriplinerve Blume Oleaceae) -
 Đánh Giá Tác Dụng Hạ Lipid Máu Dựa Trên Mô Hình Gây Tăng Cholesterol Máu Nội Sinh
Đánh Giá Tác Dụng Hạ Lipid Máu Dựa Trên Mô Hình Gây Tăng Cholesterol Máu Nội Sinh -
 Đánh giá tính an toàn và tác dụng trên các thông số lipid máu của cao chiết từ lá cây Chè vằng Jasminum subtriplinerve Blume Oleaceae trên thực nghiệm - 6
Đánh giá tính an toàn và tác dụng trên các thông số lipid máu của cao chiết từ lá cây Chè vằng Jasminum subtriplinerve Blume Oleaceae trên thực nghiệm - 6 -
 Đánh giá tính an toàn và tác dụng trên các thông số lipid máu của cao chiết từ lá cây Chè vằng Jasminum subtriplinerve Blume Oleaceae trên thực nghiệm - 7
Đánh giá tính an toàn và tác dụng trên các thông số lipid máu của cao chiết từ lá cây Chè vằng Jasminum subtriplinerve Blume Oleaceae trên thực nghiệm - 7
Xem toàn bộ 64 trang tài liệu này.

Chú thích: khác biệt so với lô chứng sinh học: *: p<0,05; **: p<0,01; ***: p<0,001.
Kết quả bảng 3.4 cho thấy: Tiêm màng bụng dung dịch P-407 2% liều 200 mg/kg có tác dụng gây RLLPM rõ rệt. Ở lô mô hình, các chỉ số TC, TG và non- HDL-C tăng có ý nghĩa so với lô chứng sinh học, khác biệt có ý nghĩa thống kê (p<0,001). Riêng HDL-C có xu hướng tăng nhưng sự tăng là không đáng kể, khác biệt không có ý nghĩa thống kê (p>0,05).
Bảng 3.5: Tác dụng của cao chiết chè vằng lên các chỉ số lipid máu của chuột nhắt trắng sau 24h tiêm P-407 (mmol/L)
n | Lô mô hình P-407 | Atorvastatin | Lô trị 1 | Lô trị 2 | |
TG | 10 | 10,76 ± 0,87 | 9,22 ± 0,33 ** (↓14,3%) | 9,91 ± 0,81 ** (↓7,9%) | 9,76 ± 0,47 ** (↓9,3%) |
TC | 10 | 7,61 ± 0,53 | 5,54 ± 0,49 *** (↓27,2%) | 6,42 ± 0,48 ** (↓15,6%) | 6,33 ± 0,40 *** (↓16,8%) |
HDL-C | 10 | 0,58 ± 0,04 | 0,54 ± 0,03 | 0,58 ± 0,03 | 0,59 ± 0,05 |
non-HDL-C | 10 | 7,03 ± 0,53 | 5,00 ± 0,50 *** (↓28,9%) | 5,84 ± 0,49 ** (↓16,9%) | 5,74 ± 0,40 *** (↓18,3%) |
Chú thích: khác biệt so với lô mô hình: *: p<0,05; **: p<0,01; ***: p<0,001.
Số liệu từ bảng 3.5 thể hiện nồng độ các chỉ số lipid máu của chuột nhắt trắng ở các lô mô hình và các lô dùng thuốc tại thời điểm 24 giờ sau khi tiêm màng bụng dung dịch P-407 gây RLLPM nội sinh.
- Cao chiết lá chè vằng liều 36 mg/kg và 108 mg/ngày và lô chứng dương (atorvastatin) đều làm giảm có ý nghĩa thống kê chỉ số TG (p <0,01), TC (p
<0,001) và non-HDL-C (p <0,001) nhưng không làm thay đổi hàm lượng HDL- C so với lô mô hình, khác biệt chưa có ý nghĩa (p >0,05).
- Giữa lô trị 1, lô trị 2 so với atorvastatin mức giảm các chỉ số TC, TG, non-HDL-C, HDL-C sự khác biệt không có ý nghĩa thống kê (p >0,05).
- Giữa lô trị 1 và lô trị 2 mức giảm các chỉ số TC, TG, non-HDL-C, HDL- C sự khác biệt không có ý nghĩa thống kê (p >0,05).
Chương 4 - BÀN LUẬN
4.1. ĐỘC TÍNH BÁN TRƯỜNG DIỄN
Nghiên cứu độc tính bán trường diễn được thực hiện bằng cách cho động vật thí nghiệm uống thuốc thử hàng ngày liên tục trong một khoảng thời gian nhất định. Trong bài nghiên cứu, khoảng thời gian được chọn cho thử nghiệm là 90 ngày. Chúng tôi tiến hành đánh giá độc tính bán trường diễn trên chuột cống trắng với 2 mức liều: liều 18 mg/kg/ngày là liều có tác dụng tương đương trên người (tính theo hệ số 6) và một liều cao hơn gấp 3 lần liều tương đương trên người (54 mg/kg/ngày), uống liên tục trong 90 ngày. Độc tính là mức độ mà một chất có thể gây hại cho con người hoặc động vật. Nó có thể tác động lên cấu trúc cơ thể , chẳng hạn như tế bào (độc tế bào), cơ quan (ví dụ: độc tính trên thận hoặc gan), hoặc toàn bộ sinh vật. Vậy để đánh giá tính an toàn của cao chiết chè vằng, chúng tôi tiến hành đánh giá một số chỉ tiêu sau:
▪ Ảnh hưởng của cao chiết về tình trạng chung, thể trọng chuột và cơ quan tạo máu: Theo hướng dẫn của WHO, tình trạng chung, trọng lượng cơ thể và các chỉ số huyết học là những xét nghiệm bắt buộc khi đánh giá độc tính của thuốc. Máu là một tổ chức quan trọng vì máu liên quan mật thiết với mọi bộ phận, cơ quan trong cơ thể [51]. Về mặt bệnh lý, máu chịu ảnh hưởng của tất cả các tổ chức đó nhưng đồng thời cũng bị ảnh hưởng và phản ánh tình trạng riêng của cơ quan tạo máu. Nếu thuốc có ảnh hưởng đến cơ quan tạo máu thì trước hết các thành phần của máu sẽ bị thay đổi, đặc biệt thường làm giảm số lượng bạch cầu. Vì vậy, các xét nghiệm về số lượng hồng cầu, số lượng bạch cầu, công thức bạch cầu, số lượng tiểu cầu trên chuột cống cần được xác định. Định lượng huyết sắc tố cho biết rõ chức năng của hồng cầu. Thể tích trung bình hồng cầu phản ánh đặc điểm của tình trạng thiếu máu. Hematocrit là tỷ lệ
% giữa khối hồng cầu và máu toàn phần [17]. Nếu thuốc làm thay đổi số lượng hồng cầu hoặc làm mất nước hay ứ nước trong tế bào máu thì chỉ số này sẽ thay đổi. Kết quả nghiên cứu cho thấy sau 30, 60 và 90 ngày nghiên cứu, trọng lượng chuột ở cả 2 lô dùng cao chiết đều tăng so với trước khi uống dịch chiết, tuy nhiên không có sự khác biệt giữa lô chứng sinh học và 2 lô dùng cao chiết. Tất cả các chỉ số huyết học ở lô chứng sinh học và cả 2 lô trị đều trong giới hạn bình thường, thay đổi không có ý nghĩa thống kê so với trước khi dùng cao
chiết và so với lô chứng sinh học ở các thời điểm sau 30, 60 và 90 ngày uống cao chiết liên tục. Như vậy, với 2 mức liều cao chiết 54 mg/kg/ngày và 108 mg/kg/ngày không làm ảnh hưởng tới sự phát triển thể trạng, cân nặng và không thể hiện độc tính trên các cơ quan tạo máu của chuột cống trắng.
▪ Ảnh hưởng của cao chiết đến chức năng gan, thận: Trong cơ thể, gan có nhiều chức năng quan trọng. Việc đưa thuốc vào cơ thể có thể gây độc với gan, làm ảnh hưởng đến chức năng của cơ quan này. Vì vậy, khi đánh giá độc tính của thuốc thì nghiên cứu ảnh hưởng của thuốc đối với chức năng gan là rất cần thiết [17]. Để đánh giá mức độ tổn thương tế bào gan, nồng độ các enzym có nguồn gốc tại gan (AST, ALT) trong huyết thanh thường được định lượng. ALT là enzym có nhiều nhất ở gan, khu trú trong bào tương của tế bào nhu mô gan. Khi tổn thương hủy hoại tế bào gan, thậm chí chỉ cần thay đổi tính thấm của màng tế bào gan, hoạt độ ALT trong máu đã tăng cao. Khác với ALT, 2/3 AST khu trú trong ty thể (mitochondria) và chỉ ít hơn 1/3 lượng AST khu trú ở bào tương của tế bào. Khi tổn thương tế bào gan ở mức độ dưới tế bào, AST trong ty thể được giải phóng ra. Vì vậy, trong viêm gan nói chung, hoạt độ ALT luôn tăng cao hơn AST. Ngoài ra, người ta còn đánh giá chức năng gan qua các chỉ số nồng độ bilirubin toàn phần, cholesterol toàn phần và albumin trong máu. Kết quả cho thấy sau 30, 60 và 90 ngày uống cao chiết, các chỉ số hoạt độ AST, ALT, nồng độ bilirubin toàn phần, cholesterol toàn phần và albumin trong máu không thay đổi có ý nghĩa so với lô chứng và so sánh giữa hai thời điểm trước và sau khi uống các liều cao chiết. Thận là cơ quan bài tiết của cơ thể, nhu mô thận rất dễ tổn thương bởi các chất nội sinh và ngoại sinh vì là mô có nhiều máu qua nhất. Vì vậy, khi đưa thuốc vào cơ thể thuốc có thể gây tổn thương thận, từ đó ảnh hưởng đến chức năng thận [51]. Creatinin là thành phần đạm trong máu ổn định nhất, hầu như không phụ thuộc vào chế độ ăn hoặc những thay đổi sinh lý mà chỉ phục thuộc vào khả năng đào thải của thận. Khi cầu thận bị tổn thương, nồng độ creatinin máu tăng sớm hơn ure. Do vậy, creatinin máu là chỉ tiêu tin cậy và quan trọng hơn ure máu, nên hiện nay dùng để đánh giá và theo dõi chức năng thận [17]. Kết quả nghiên cứu cho cao chiết chè vằng ở cả 2 liều khi dùng đường uống trên chuột cống liên tục trong 90 ngày không làm thay đổi nồng độ creatinin so với lô chứng sinh học.
▪ Ảnh hưởng của cao chiết lên cấu trúc đại thể và vi thể: Theo hướng dẫn của WHO, giải phẫu đại thể và vi thể gan thận là chỉ số bắt buộc khi đánh giá độc tính bán trường diễn. Ngoài ra, xét nghiệm vi thể còn là tiêu chuẩn vàng để đánh giá tổn thương 2 cơ quan chính chịu trách nhiệm chuyển hóa và thải trừ thuốc là gan và thận [51]. Trên tất cả chuột nghiên cứu, không quan sát thấy có thay đổi bệnh lý nào về mặt đại thể của các cơ quan. Kết quả giải phẫu bệnh cho thấy cao chiết chè vằng cả 2 liều khi dùng đường uống trên chuột cống liên tục trong 90 ngày không làm thay đổi hình ảnh mô bệnh học thận so với lô chứng sinh học.
Hình ảnh vi thể gan không có sự khác biệt giữa lô chứng và các lô uống cao chiết chè vằng. Quan sát ngẫu nhiên cấu trúc vi thể gan của 30% số chuột kết quả cho thấy mẫu bệnh phẩm gan có hình ảnh thoái hóa nhẹ (lô trị 1) đến thoái hóa vừa (lô trị 2) tế bào gan. Tại gan, khi các nguyên nhân gây tổn thương tấn công, các tế bào gan có thể bị ảnh hưởng nặng hoặc nhẹ tùy thuộc vào loại nguyên nhân và thời gian tiếp xúc với nguyên nhân tổn thương. Sự tổn thương của tế bào nói chung và tế bào gan nói riêng được chia làm 3 mức độ khác nhau là tổn thương có khả năng hồi phục (thoái hóa), tổn thương có nguy cơ gây chết tế bào và tổn thương không có khả năng hồi phục (hoại tử) [15]. Trong các tổn thương tế bào nói trên, tổn thương thoái hóa là tổn thương ban đầu và nhẹ nhất của tế bào, các tế bào có thể tự phục hồi lại được tổn thương này để trở về tình trạng bình thường. Sự thoái hóa của tế bào có thể là thoái hóa hạt, thoái hóa nước và thoái hóa mỡ. Kết hợp với kết quả xét nghiệm đánh giá tổn thương tế bào gan, hoạt độ ALT và AST ở 2 lô uống cao chiết chè vằng đều ở mức bình thường, không khác biệt so với lô chứng, nên theo nhóm nghiên cứu, chưa có cơ sở để cho rằng cao chiết chè vằng gây tổn thương gan chuột thông qua xét nghiệm vi thể gan chuột tại nghiên cứu độc tính bán trường diễn.
Từ đó có thể kết luận rằng cao chiết lá chè vằng (Jasminum subtriplinerve Blume Oleaceae) có tính an toàn.
4.2. HIỆU QUẢ ĐIỀU TRỊ RỐI LOẠN LIPID MÁU CỦA CAO CHIẾT LÁ CHÈ VẰNG (Jasminum subtriplinerve Blume Oleaceae) TRÊN CÁC THÀNH PHẦN LIPID MÁU
4.2.1. Đánh giá mô hình tăng lipid máu nội sinh bằng P-407
Trong nghiên cứu này, chúng tôi chọn P-407 liều 200 mg/kg tiêm màng bụng để gây RLLPM nội sinh trên chuột nhắt trắng, atorvastatin liều 100 mg/kg được sử dụng làm thuốc đối chứng. Atorvastatin và cao chiết được uống kéo dài 7 ngày trước khi gây mô hình. Poloxamer 407 là một chất hoạt động bề mặt không ion hóa có khả năng gây RLLPM thông qua một số cơ chế liên quan đến các enzym tham gia vào quá trình chuyển hóa lipid [37]. Mô hình nội sinh được thực hiện bằng cách dùng các chất hoạt động bề mặt không ion hoá như Tween 80, Triton WR-1339 hoặc Poloxamer 407 (P-407) đường toàn thân mà không cần dùng tới nguồn lipid ngoại sinh bổ sung bằng đường ăn uống. Các chất này đã được chứng minh cơ chế làm tăng tổng hợp cholesterol tại gan [23, 41]. Trước đây, nhóm nghiên cứu đã sử dụng Tween 80 để gây rối loạn lipid máu nhưng kết quả thu được không ổn định, không làm rối loạn rõ rệt nồng độ lipid máu của động vật thí nghiệm. Ở nghiên cứu này, chúng tôi chọn P- 407 vì có khả năng gây tăng lipid máu cao hơn và an toàn hơn so với Triton WR-1339 [31, 41]. Tham khảo liều dùng P-407 trên chuột nhắt trắng từ các nghiên cứu trước [24, 25, 41] trong nghiên cứu này liều P- 407 được dùng là 200 mg/kg chuột. Sau khi tiêm màng bụng chuột, nồng độ lipid máu bắt đầu tăng và đạt cực đại sau 24 giờ, sau đó giảm dần về bình thường [24, 38], do vậy chúng tôi chọn thời điểm 24 giờ sau khi tiêm P- 407 để định lượng nồng độ lipid máu của chuột thí nghiệm.
Kết quả nghiên cứu trong bảng 3.4 cho thấy, ở các lô được tiêm màng bụng P- 407, tất cả các thông số lipid máu đều tăng lên rõ rệt so với lô chứng sinh học, trong đó tăng cao nhất là nồng độ TG (gấp khoảng 8 lần so với nhóm chứng), nồng độ TC và nồng độ non-HDL-C tăng ít hơn, gấp khoảng 3 lần so với nhóm chứng sinh học. Tất cả chuột ở các lô sau khi được tiêm P-407 đều không có dấu hiệu bất thường nào về tình trạng chung như: chuột vẫn hoạt động bình thường, nhanh nhẹn, mắt sáng, lông mượt, phân khô, không có chuột nào chết. Điều đó cho thấy P-407 là một chất có hiệu quả và an toàn trong việc gây mô
hình rối loạn lipid máu nội sinh trên động vật thí nghiệm. Kết quả này tương đối phù hợp với các nghiên cứu trước đó tiến hành trên chuột nhắt trắng [24, 31, 41], mặc dù mức tăng chỉ số TG thấp hơn so với mô hình của tác giả Phạm Thanh Tùng, Đỗ Quốc Hương và Tạ Thu Thủy nhưng cũng đã thể hiện được mức tăng đáng kể các chỉ số lipid máu, mức tăng có ý nghĩa thống kê (p < 0,001 với TC, TG và non-HDL-C) [16, 26, 28]. Vì vậy, mô hình tăng lipid máu bằng P-407 trong nghiên cứu là thành công.
4.2.2. Đánh giá mô hình thuốc đối chứng Atorvastatin 10 mg
Trên mô hình nghiên cứu thực nghiệm, thuốc đối chứng được lựa chọn là viên nén atorvastatin 10 mg. Đây cũng là loại thuốc thường được các nhà nghiên cứu trên thế giới sử dụng làm thuốc đối chứng. Atorvastatin là thuốc thuộc nhóm statin, là nhóm hiệu quả nhất trong điều trị rối loạn lipid máu hiện nay với cơ chế ức chế enzym HMG-CoA reductase, làm giảm tổng hợp cholesterol và làm tăng hoạt động của các LDL receptor ở gan. Về tác dụng của thuốc trong nhóm statin thì mức độ điều chỉnh RLLPM giảm dần theo thứ tự: Rosuvastatin, atorvastatin, simvastatin, lovastatin,…[53]. Do đó sử dụng rosuvastatin làm thuốc chứng dương sẽ có kết quả tốt nhất, tuy nhiên giá thành rosuvastatin đắt, mà atorvastatin có tác dụng khá tốt, nên chúng tôi chọn atorvastatin làm thuốc đối chứng để so sánh.
Trong nghiên cứu chúng tôi chọn mức liều cao là 100 mg/kg vì trên lâm sàng thuốc điều trị RLLPM thường bắt đầu có tác dụng sau 10 – 15 ngày và tối đa sau 1 tháng. Trong khi đó thời gian thực hiện trên mô hình nội sinh là 7 ngày nên phải chọn liều cao mới có thể đánh giá được tác dụng điều chỉnh RLLPM.
P-407 là một chất hoạt động bề mặt (chất hoạt động bề mặt) dựa trên polyether, cung cấp một phương tiện gây tăng lipid máu do nó khởi phát nhanh và dường như không có độc tính quá mức so với Triton WR-1339 [40]. Poloxamer 407 có được biết là gây tăng cholesterol máu phụ thuộc vào liều đáng kể và tăng triglycerid máu ở chuột cống và chuột nhắt theo một số cơ chế (ức chế lipoprotein lipase, kích thích gián tiếp HMG-CoA (3-hydroxy-3- methylglutaryl Co-A) reductase, thúc đẩy nồng độ cholesterol ở gan). Dựa trên cơ chế của P-407 và các mảnh bằng chứng về hiệu quả, statin được chọn làm